This cruise was the final of four from the project «VDWS». The project aimed to assess the sensitivity of management-relevant cold-water species to aquaculture emissions and to develop methods for monitoring impacts on health condition. Seven ROV dives were conducted on 16–17 August 2025 to collect and visually assess the health condition of selected benthic species around a salmon aquaculture facility in the Nordland region. Target species included Acesta excavata, Primnoa resedaeformis, Paragorgia arborea, Phakellia ventilabrum, and Geodia barretti. A total of 39 samples were collected, primarily to test and optimize the Lysosomal Membrane Stability (LMS) protocol for assessing the target species’ sensitivity to aquaculture emissions, and to acquire live fragments of the coral Desmophyllum pertusum for planned exposure experiments. In addition, Visual health assessments were performed and correlated with LMS results.
Metodetesting for å vurdere følsomheten hos forvaltningsrelevante bunnarter til akvakulturutslipp
— Toktrapport 2025005014
Rapportserie:
Toktrapport 2026-8
ISSN: 1503-6294
Publisert: 09.03.2026
Forskningsgruppe(r):
Bentisk økologi
Program:
Miljøeffekter av akvakultur
Forskningsgruppeleder(e):
Vivian Husa (Bentisk økologi)
Godkjent av:
Forskningsdirektør(er):
Geir Lasse Taranger
Programleder(e):
Mari Skuggedal Myksvoll
English summary
Sammendrag
Dette toktet var det siste av fire fra prosjektet «VDWS». Prosjektets mål var å vurdere følsomheten hos forvaltningsrelevante dypvannsarter for utslipp fra akvakultur, og å utvikle metoder for å overvåke påvirkning på helsetilstand. Sju ROV-dykk ble gjennomført 16. til 17. august 2025 for å samle inn prøver og visuelt vurdere helsetilstand hos utvalgte bunndyrsarter rundt et lakseoppdrettsanlegg i Nordland. Disse målartene inkluderte bergskjell (Acesta excavata), risengrynkorall (Primnoa resedaeformis), sjøtre (Paragorgia arborea), viftesvamp (Phakellia ventilabrum) og kålrabisvamp (Geodia barretti). Totalt 39 prøver ble samlet, primært for å teste og optimalisere lysosomal membranstabilitet (LMS)-protokollen for å vurdere målartenes følsomhet for utslipp fra akvakultur, samt for å innhente levende fragmenter av øyekorall (Desmophyllum pertusum) for planlagte eksponeringforsøk. I tillegg ble visuell helsevurdering gjennomført, og disse observasjonene ble korrelert med LMS-data.
1 - Bakgrunn
Overvåking av bunndyrs følsomhet for påvirkning fra lakseoppdrett er viktig for forvaltning og bevaring. Dette prosjektet fokuserte på kaldtvannsarter som ofte er langsomtvoksende og sårbare for fysisk og kjemisk forstyrrelse. Målarter inkluderte bergskjell (Acesta excavata), risengrynkorall (Primnoa resedaeformis), sjøtre (Paragorgia arborea), viftesvamp (Phakellia ventilabrum), kålrabisvamp (Geodia barretti) og øyekorall (Desmophyllum pertusum).
Lysosomal membranstabilitet (LMS) er et tidlig og sensitivt mål på cellulært stress, og brukes som indikator på miljøpåvirkning fra sediment, kjemikalier eller temperaturendringer for en rekke marine arter. LMS har tidligere vist seg å være nyttig for å vurdere helse hos svamper, koraller og bergskjell under eksponering for oppdrettsrelaterte påvirkninger (f.eks. Mamaca mfl. (2005); Edge mfl. (2014); Edge mfl. (2016); Mukherjee mfl. (2015); Strand mfl. (2017); Kutti mfl. (2022)).
Hensikten med dette prosjektet var å teste og videreutvikle LMS-protokollen for norske kaldtvannsarter, samle levende prøver for laboratorieforsøk, samt utføre visuelle helsevurderinger for å evaluere følsomheten til forvaltningsrelevante bunndyr overfor oppdrettsaktiviteter.
2 - Metoder
2.1 - Toktdesign og prøvetakning
Siste tokt i VDWS-prosjektet ble gjennomført fra 15. til 18. august 2025 i Sagfjorden, med Havforskningsinstituttet (HI) sitt kystfartøy Prinsesse Ingrid Alexandra (PIA). Fra HI deltok Katherine M. Dunlop, Mona M. Fuhrmann og Ana S. Gomes som toktdeltakere.
Stasjonsposisjoner for VDWS-prosjektet ble fastsatt på forhånd basert på tidligere overvåkingsaktiviteter og prøvertaking på tidligere tokt fra prosjektet. Visuelle ROV-undersøkelser dokumenterte forekomst av korallrev, korallskog og svampskog i avstander fra < 50 til > 500 m fra lokalitetene. I tillegg bekreftet ROV-undersøkelser gjennomført i 2023 og 2024 (tokt 2023005005 og 2024005025) tilstedeværelsen av målartene, og biologiske prøver ble også samlet inn under disse toktene.
Fokuset var rettet mot oppdrettsanleggene i Økssundet, som ligger i kommunene Hamarøy og Steigen i Nordland. Området er karakterisert av bratte fjordsider, komplekst bunnrelieff og har et maksimumsdyp på 630 m. Lokalitetene Oksøy (11320) og Anevik (30156) ligger på østsiden av Lundøya i Økssundet og ble etablert i henholdsvis 1999 og 2009. Begge lokalitetene produserer atlantisk laks med en maksimal biomasse på 5400 tonn. Mellom 2015 og 2020 ble azametifos og emamektin benyttet til lusebehandling ved både Oksøy og Anevik, i tillegg til bruk av rensefisk ved Anevik. Etter 2020 har azametifos, emamektin og også hydrogenperoksid blitt brukt ved begge lokalitetene, mens Horsvågen har benyttet emamektin i tillegg til mekanisk og termisk avlusning.
Studiedesignet var lagt opp for å undersøke helsetilstand av målarter langs en romlig anrikningsgradient, fra områder nærmest oppdrettsmerdene og ut til referanseområder på avstander større enn 1 km. Målet var å sikre sammenlignbare innsamlingspunkter langs denne gradienten. Totalt ble det gjennomført sju dykk med HIs ROV Freyja (Argus Remote Systems, modell Mariner 141) på dyp mellom 177 og 403 m. Visuelle observasjoner ble utført med et Sony FCB-EV7520A-kamera (uten direktestrøm) montert i omtrent 60° vinkel, som ble verifisert ved start av hver stasjon og holdt konstant under transektene. To lasere med 10 cm innbyrdes avstand ble brukt for skalering av objekter. Posisjonering ble utført ved hjelp av HIPAP-systemer (HiPAP 502 for Minerva og µPAP 200 med Cnode mini S-transponder for Freyja). Høyden over bunnen ble overvåket med altimeter, og holdt på omtrent 1 m under videoregistreringen. Prøver ble deretter samlet inn ved bruk av ROV-ens gripeverktøy. Under videoregistrering og prøvetaking (Figur 1) ble posisjonene av aktuell aktivitet registrert med SeaBed Field Observer SFO-systemet. For å sikre systematisk dokumentasjon av bentiske arter ble en standardisert protokoll fulgt, der det det ble tatt bilder i fast rekkefølge: først et oversiktsbilde av det bentiske samfunnet og omkringliggende arter, deretter et bilde av individet alene som fyller hele kamerafeltet, og til slutt et nærbilde av vevet.
Under prøvetaking ble korallfragmenter ble klippet fra hovedkolonien ved bruk av manipulatorarmen (Figur 1), mens svamper ble samlet inn som hele individer. Bergskjell ble samlet inn med en spesialdesignet skje som reduserte risikoen for skade på skall og bløtvev. Innsamlingen omfattet bergskjell, risengrynkorall, sjøtre, viftesvamp og kålrabisvamp, og hadde tre hovedformål: (i) å teste og optimalisere protokollen for lysosomal membranstabilitet (LMS) som indikator på målartenes følsomhet for påvirkning fra akvakulturutslipp, (ii) å gjennomføre visuelle helsevurderinger av de samme individene, og (iii) å undersøke sammenhenger mellom visuelle tegn på påvirkning og fysiologiske responser målt ved LMS. Etter innsamling ble prøvene oppbevart i sjøvann frem til videre prosessering, og hvert individ ble fotografert i laboratoriet før videre prøvetaking og analyser (Figur 1). I tillegg ble levende fragmenter av øyekorall samlet inn til planlagte eksponeringsforsøk.

2.2 - Lysosomal membranstabilitet (LMS) protokoll
Lysosomal membranstabilitet (LMS) ble vurdert ved bruk av nøytralrød-assay, basert på en forenklet protokoll av Edge mfl. (2014, 2015, 2016) etter Lowe mfl. (1992) og Ringwood mfl. (1998, 2005). Metoden er basert på opptak og retensjon av fargestoffet nøytralrød i intakte lysosomer, og brukes som et mål på cellestabilitet. Assayet ble anvendt på vev fra svamper, koralldyr, samt hemolymfe fra bergskjell. Vi testet ulike vevshåndterings- og prosesseringsbetingelser for de studerte artene (Tabell 1).
Vevsprøver ble oppbevart i kaldt sjøvann og mørke frem til bearbeiding. Dissosiasjon av vevet til enkeltceller ble utført i Ca²⁺/Mg²⁺-fri saltløsning (CMFS: 20 mM HEPES, 360 mM NaCl, 12,5 mM KCl, 5 mM EDTA, pH 8,0). Vevet (ca. 1 cm) ble kuttet i små biter på objektglass (svamper og koraller) eller knust med morter og pistill (koraller) og deretter overført til 24-brønns cellekulturplater (Figur 2). Vevshåndtering, homogenisering og prosesseringsbetingelser varierte noe mellom arter (Tabell 1). Hemolymfe fra bergskjell ble samlet inn ved bruk av en 1 mL sprøyte med en 21G nål (0,8 × 40 mm). Omtrent 100 µL hemolymfe ble tatt ut, og nålen fjernet fra sprøyten før prøven ble overført til et rør, slik at cellene ikke ble mekanisk ødelagt. Av dette ble 50 µL brukt videre til bearbeiding.
| Art | Testede betingelser | Vevshomogenisering | Porestørrelse | Volum | Temperatur |
|---|---|---|---|---|---|
| Bergskjell | Inkubasjonstemperatur | N/A | N/A | 50 µL | 4 °C / RT |
| Viftesvamp | Masketype; Inkubasjonstemperatur | Skåret i små biter | 40 µm | 50 µL | 4 °C / RT |
| Kålrabisvamp | Resuspensjonsvolum | Skåret i små biter | 40 µm | 50 µL / 100 µL | RT |
| Risengrynkorall | Vevsforberedelse; Porestørrelse | Knust vs Skåret i små biter | 70 µm / 100 µm | 50 µL | RT |
| Sjøtre | Vevsforberedelse; Porestørrelse; Resuspensjonsvolum | Knust vs Skåret i små biter | 70 µm / 100 µm | 50 µL / 150 µL | RT |
Prøvene ble inkubert i mørke ved 4 °C i 30 minutter. Etter inkubasjon ble cellene forsiktig separert ved skånsom opp- og nedpipettering med en modifisert Pasteur-pipette (avknekt spiss). Celleoppløsningen ble filtrert gjennom artsspesifikke nylonporestørrelser (40–100 µm). To filtreringsmetoder ble testet: et hjemmelaget filter av planktonduk montert i en modifisert 1000 µL pipettespiss, og en kommersiell cellesil (VWR). Den hjemmelagde silen tettet seg ofte, mens VWR-silen, med større filtreringsflate, gjorde filtreringen enklere og mer effektiv. Etter filtrering ble celleoppløsningen sentrifugert ved 2000 g i 5 minutter. Den ble vasket én gang med kald CMFS og sentrifugert på nytt under samme betingelser. Til slutt ble cellene samlet i bunnen av røret (pellet) og resuspendert i 50 µL CMFS (50 eller 100 µL for kålrabisvamp og 50 eller 150 µL for sjøtre).
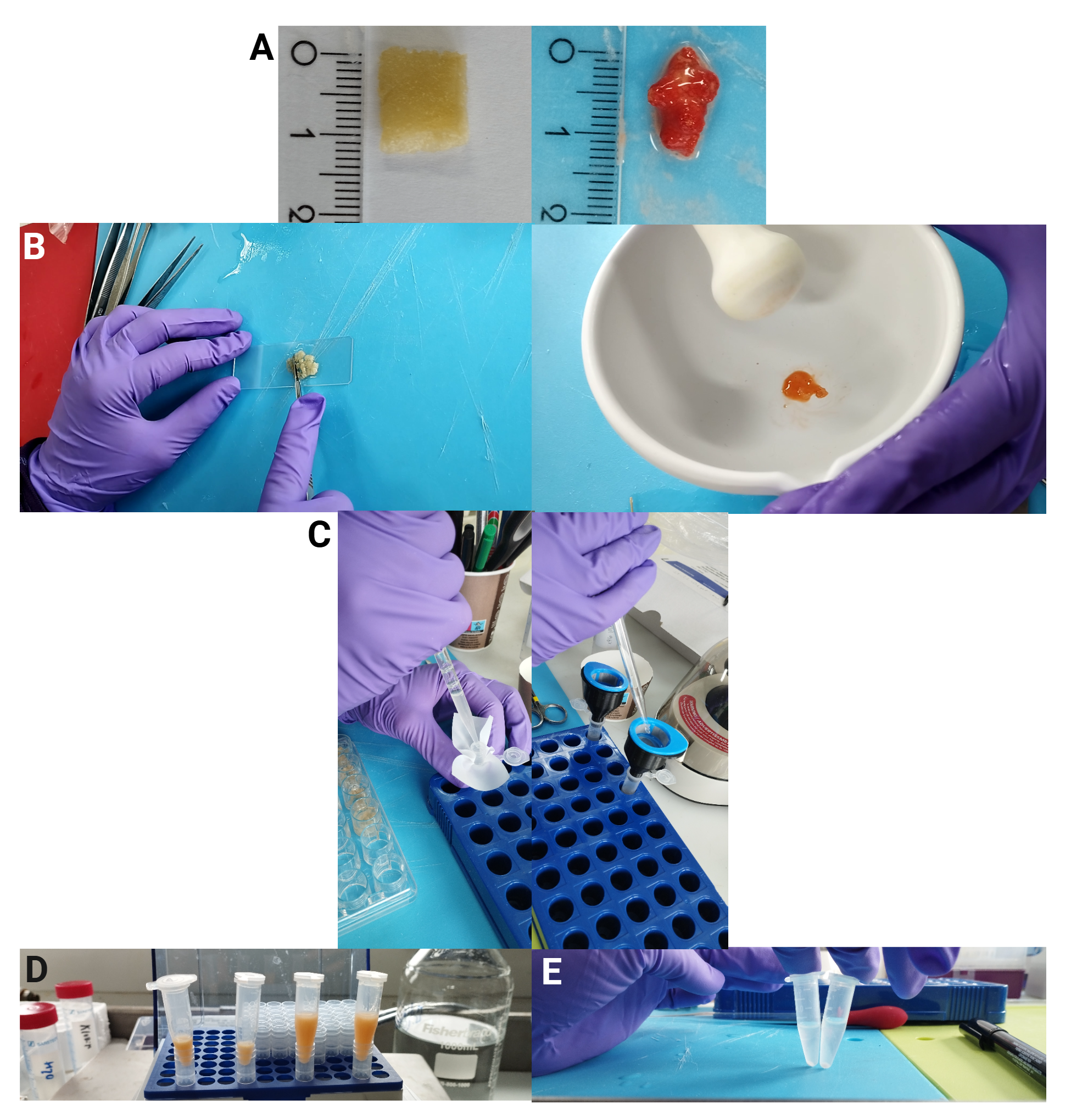
En nøytralrød-arbeidsløsning (0,08 mg·L⁻¹) ble klargjort daglig, og tilsatt celleoppløsningen i samme volum som CMFS (forhold 1:1). Etter forsiktig blanding ble prøvene inkubert i mørke ved 4 °C eller ved romtemperatur (RT, ca. 15 °C) i 60 minutter. Rett før vurdering ble 20 µL av resuspenderte cellene overført til et objektglass.
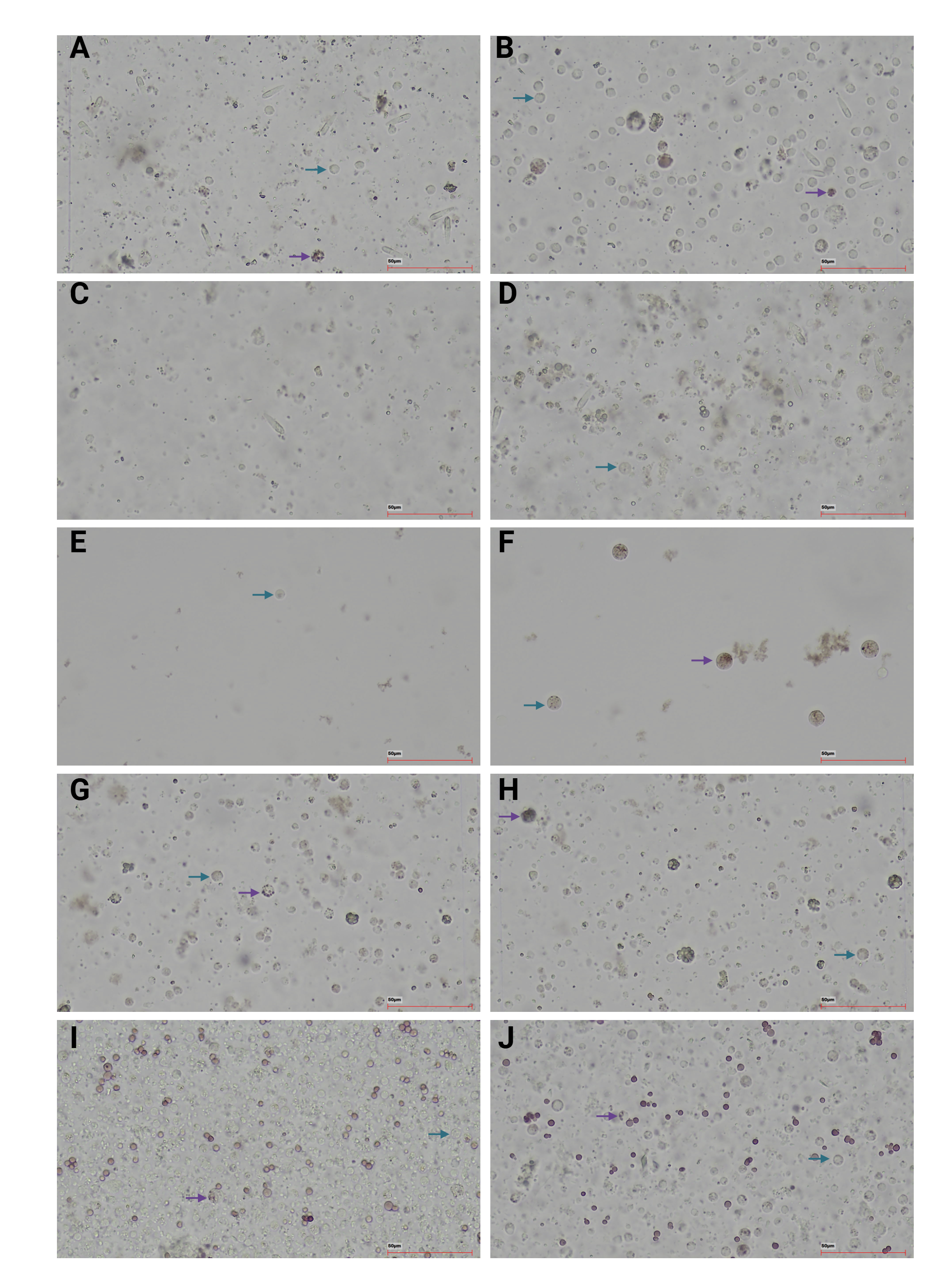
Minst 50 celler per prøve ble vurdert under mikroskop med 40×-objektiv. Celler ble kategorisert som stabile (nøytralrød beholdt i lysosomene) eller ustabile (nøytralrød lekket til cytoplasma). Prosentvis stabilisering ble beregnet som andelen stabile celler av totalt observerte celler. Representativ observasjon av cellene per art vises i Figur 3.
2.3 - Visuell helseevaluering
Helsetilstanden hos målartene ble vurdert ved bilder tatt in situ med ROV, samt ved bilder tatt av prøver i laboratoriet. Helsekriterier inkluderte vevsskade, bleking og begroing. Kriterier for hver art (hornkorall, bergskjell og svamp) ble dokumentert og brukt til å generere en helseindeks.
3 - Resultater
3.1 - Stasjonsoversikt
Totalt ble sju ROV-dykk gjennomført, hvorav fire ved referanseområder og tre i nær tilknytning til oppdrettslokaliteten Anevik.

Prøvetakingsinnsatsen varierte mellom ROV-dykkene med hensyn til dybdeintervall, avstand til oppdrettslokaliteter og antall innsamlede prøver (Tabell 2). Referansedykkene (dykk 356, 357, 358 og 362) ble gjennomført i avstander mellom ca. 2,0 og 3,8 km fra Anevik, og mellom ca. 1,3 og 1,9 km fra Oksøy (ikke i produksjon på tidspunktet for prøvetakingen). Dybdeintervallene for disse dykkene strakte seg fra 275 til 401 m. Antall prøver per referansedykk varierte fra 3 til 14, med tap kun registrert i dykk 356 (4 tapte prøver). Prøvetapet skjedde under oppstigning av ROV-en til fartøyet, da enkelte prøver ikke var fullstendig sikret i prøveskuffen og ble mistet før ankomst til dekk.
Nær-anlegg-dykkene (dykk 359–361) ble gjennomført i umiddelbar nærhet til Anevik, med avstander mellom 93 og 139 m. Dybdeintervallene varierte mellom 251 og 320 m, og antall prøver per dykk varierte fra 4 til 7, uten registrerte prøvetap.
| Dykknr | Områdetype | Avstand til Anevik (m) | Avstand til Oksøy (m) | Dybde (m) | Prøver (tapt) |
|---|---|---|---|---|---|
| 356 | Referanse | 2031–2080 | 1347–1358 | 316–401 | 14 (4) |
| 357 | Referanse | 3774–3789 | 1910–1935 | 275–349 | 7 (0) |
| 358 | Referanse | 3757–3768 | 1904–1905 | 356–361 | 3 (0) |
| 359 | Nær anlegg | 93–113 | – | 251–320 | 7 (0) |
| 360 | Nær anlegg | 103–105 | – | 300–302 | 4 (0) |
| 361 | Nær anlegg | 131–139 | – | 277–282 | 5 (0) |
| 362 | Referanse | 3765–3767 | 1899–1908 | 357–361 | 3 (0) |
3.2 - Prøveoversikt
Antall innsamlede prøver per art og lokalitetstype fremgår av Tabell 3 (for detaljert informasjon, se Vedlegg A1). Artene med flest innsamlede prøver var bergskjell og risengrynkorall. Viftesvamp var mindre representert, og Phakellia robusta ble samlet ved en feil, da den først ble feilidentifisert som viftesvamp. Det ble kun én prøve av viftesvamp observert og samlet nær Anevik, noe som tyder på at arten er mindre vanlig i dette området sammenlignet med referanseområdene. Der ble tre prøver av viftesvamp samlet, i tillegg til to prøver som gikk tapt under transport fra ROV-bunnen til fartøyet. Dette kan indikere at viftesvamp er mer sensitiv for påvirkning fra oppdrett, eller at dette habitatet ikke er optimalt for arten. Øyekorall ble kun samlet i referanseområder for et planlagt laboratorieforsøk ved NORD Universitet.X
| Art | Nær anlegg | Referanseområde |
|---|---|---|
| Bergskjell | 4 | 4 |
| Kålrabisvamp | 3 | 3 |
| Phakellia robusta | 2 | 0 |
| Risengrynkorall | 3 | 3 |
| Sjøtre | 3 | 3 |
| Viftesvamp | 1 | 3 |
| Øyekorall | 0 | 7 |
3.3 - Lysosomal membranstabilitet
Under dette toktet hadde vi som mål å videreutvikle LMS-protokollen for vev fra svamper og koraller, samt for hemolymfe fra bergskjell. Det ble gjennomført tester for å evaluere metoder for vevshomogenisering, filtertype (hjemmelagde filtre versus kommersielle cell strainere) og porestørrelse, resuspensjonsvolum samt inkubasjonstemperatur under farging med nøytralrød.
Når det gjelder vevshomogenisering, ble det observert tydelige arts-spesifikke forskjeller. For sjøtre ga kutting av vevet i små biter høyere celleutbytte enn knusing av vevet (se Figur 2 panel D, der de to første rørene med knust vev viser et betydelig lavere cellevolum sammenlignet med de to siste rørene med kuttet vev). En mulig forklaring på denne forskjellen er det høye sliminnholdet i vevet hos sjøtre, som kan føre til tilstopping av filtrene under filtrering. For risengrynkorall ga knusing av vevet med morter og pistill bedre resultater. Samlet sett viste bruk av kommersielle cell strainere seg å være mer effektivt enn hjemmelagde filtre, hovedsakelig på grunn av større effektiv filterflate, som ga mer effektiv filtrering av prøvene (Figur 2 panel E). For risengrynkorall bidro bruk av 100 µm filter til renere preparater på objektglass (Figur 3 panel A og B). For bergskjell var inkubasjon med nøytralrød ved romtemperatur (RT, ca. 15 °C) under det avsluttende fargetrinnet nødvendig for å oppnå tilstrekkelig fargeopptak. For sjøtre og kålrabisvamp forbedret resuspensjon av cellene i henholdsvis 100 og 150 µL CMFS, etterfulgt av tilsetning av et tilsvarende volum nøytralrød-arbeidsløsning, håndtering av prøvene og identifikasjon av celler.
Basert på de samlede resultatene fra disse testene ble arts-spesifikke LMS-protokoller etablert og er oppsummert i Vedlegg A2.
3.3.1 - LMS for ulike arter
LMS-stabiliteten varierte mellom arter og mellom lokaliteter nær oppdrettsanlegg og referanseområder (Tabell 4). For bergskjell var gjennomsnittlig stabilitet lav nær anleggene (16 ± 6 %) og betydelig høyere i referanseområdene (61 ± 24 %). Kålrabisvamp hadde høy stabilitet både nær anlegg og i referanseområder (87 ± 7 % vs. 91 ± 8 %). Risengrynkorall hadde kun én prøve nær anlegg (40 %), sammenlignet med 75 ± 12 % i referanseområdet. Sjøtre ble kun samlet inn nær anlegg, med en gjennomsnittlig LMS på 73 ± 33 %. Viftesvamp viste lav stabilitet nær anleggene (24 %), mens referanseområdene hadde svært høy stabilitet (97 ± 3 %). Resultatene antyder generelt lavere LMS-stabilitet nær oppdrettsanlegg for enkelte arter, mens andre var stabile på tvers av lokalitetstyper. Ettersom antallet prøver generelt er lavt for flere arter må resultatene tolkes med forsiktighet.
| Art | Nær anlegg (n) | Referanseområde (n) | Nær anlegg (gj.sn. ± SD %) | Referanseområde (gj.sn. ± SD %) |
|---|---|---|---|---|
| Bergskjell | 4 | 3 | 16 ± 6 | 61 ± 24 |
| Kålrabisvamp | 3 | 3 | 87 ± 7 | 91 ± 8 |
| Risengrynkorall | 1 | 3 | 40 ± NA | 75 ± 12 |
| Sjøtre | 3 | 0 | 73 ± 33 | - |
| Viftesvamp | 1 | 3 | 24 ± NA | 97 ± 3 |
3.4 - Helseindeks for arter nær anlegg og i referanseområder
Helseindeksen for de innsamlede artene, der 0 representerer intakt prøve og 2 mest nedbrutt prøve, varierte både mellom arter og mellom lokaliteter nær oppdrettsanlegg og referanseområder (Tabell 5). For bergskjell var gjennomsnittlig helseindeks 1,33 ± 0,39 nær anlegg og 0,50 ± 0,34 i referanseområder, noe som indikerer mer nedbrutte prøver nær anleggene. Kålrabisvamp hadde generelt lave helseindekser, med 0,33 ± 0,38 nær anlegg og 0,25 ± 0 i referanseområder. Risengrynkorall viste høyere verdier nær anlegg (1,08 ± 0,29) sammenlignet med referanseområder (0,50 ± 0). Sjøtre hadde en gjennomsnittlig helseindeks på 1,22 ± 0,51 nær anlegg, mens alle prøver i referanseområder hadde verdi 0. For viftesvamp var helseindeksen 0,80 nær anlegg (n = 1) og 0,47 ± 0,31 i referanseområder. Totalt sett hadde prøver nær oppdrettsanlegg en tendens til å ha høyere helseindeks, som indikerer en dårligere helsetilstand, enn prøver fra referanseområder, noe som kan indikere økt stress eller nedbrytning. På grunn av lavt prøveantall for flere arter, særlig for viftesvamp nær anlegg, bør disse mønstrene tolkes med stor forsiktighet og inngå i et større datasett for å analysere effekter av utslipp.
| Art | Nær anlegg (n) | Referanseområde (n) | Nær anlegg (gj.sn. ± SD) | Referanseområde (gj.sn. ± SD) |
|---|---|---|---|---|
| Bergskjell | 4 | 4 | 1.33 ± 0.39 | 0.50 ± 0.34 |
| Kålrabisvamp | 3 | 3 | 0.33 ± 0.38 | 0.25 ± 0.00 |
| Risengrynkorall | 3 | 3 | 1.08 ± 0.29 | 0.50 ± 0.00 |
| Sjøtre | 3 | 3 | 1.22 ± 0.51 | 0.00 ± 0.00 |
| Viftesvamp | 1 | 3 | 0.80 ± NA | 0.47 ± 0.31 |
3.5 - Sammenheng mellom LMS og helseindeks
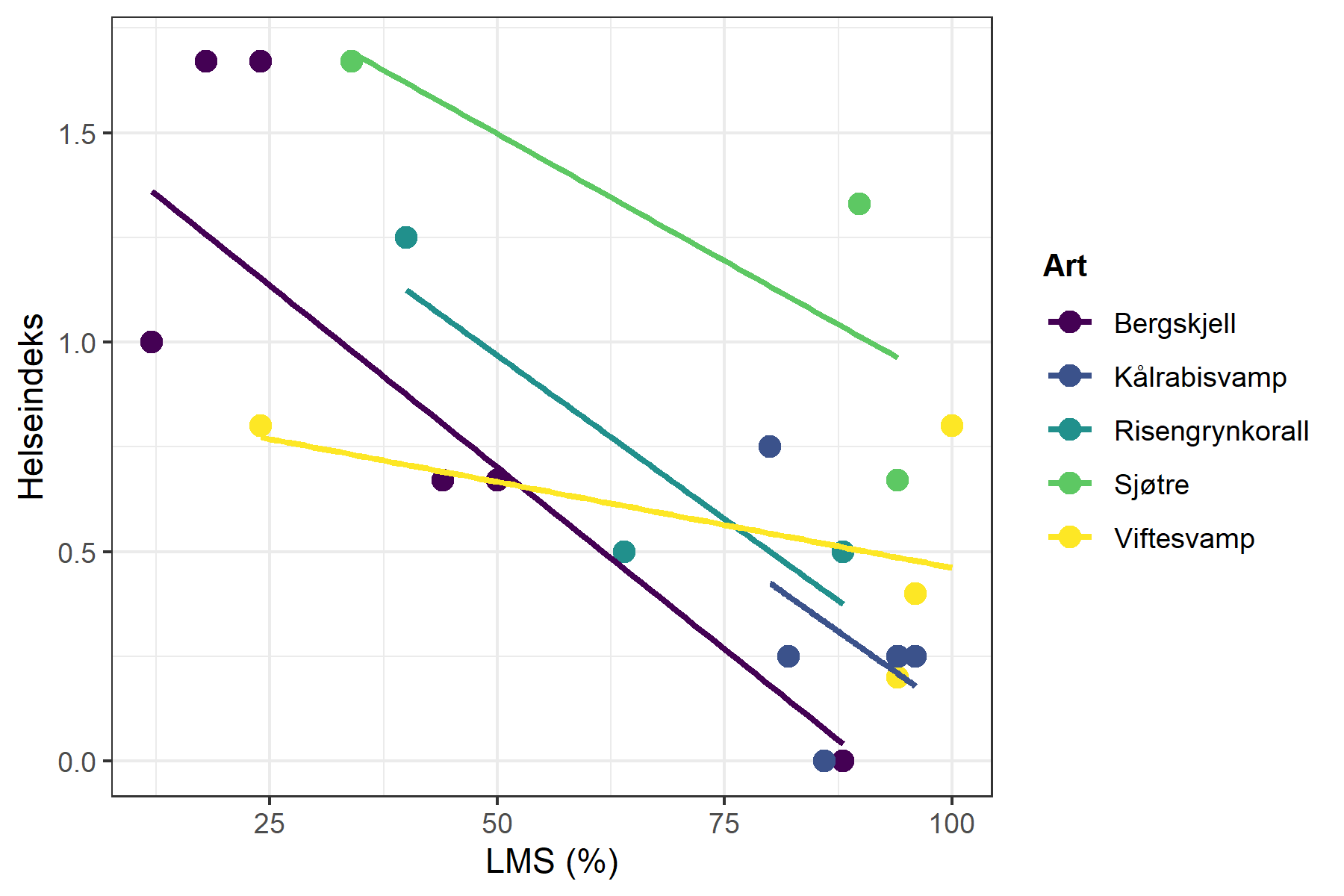
Den overordnede sammenhengen mellom LMS og helseindeks er også vist grafisk i Figur 5. Spearman-rangkorrelasjoner mellom LMS (% stabiliserte celler) og helseindeks ble beregnet for hver art der minst tre prøver var tilgjengelige (Tabell 6). Bergskjell viste en moderat negativ korrelasjon (r = −0,69, n = 7), noe som indikerer at prøver med høyere LMS (flere stabiliserte celler) hadde lavere (bedre) helseindeks. Kålrabisvamp viste en svak negativ korrelasjon (r = −0,34, n = 6). Risengrynkorall viste en sterk negativ korrelasjon (r = −0,87, n = 3), mens Sjøtre viste en svært sterk negativ korrelasjon (r = −1,00, n = 3). Viftesvamp skilte seg ut med en svært svak positiv korrelasjon (r = 0,11, n = 4). Samlet sett indikerer resultatene at høyere LMS (flere stabiliserte celler) for de fleste arter samsvarer med bedre visuell helse. Styrken på sammenhengen varierer imidlertid mellom arter og må tolkes med stor forsiktighet på grunn av lave prøvetall, særlig for arter med kun tre tilgjengelige prøver.
| Art | Antall prøver (n) | Spearman korrelasjon |
|---|---|---|
| Bergskjell | 7 | -0,69 |
| Kålrabisvamp | 6 | -0,34 |
| Risengrynkorall | 3 | -0,87 |
| Sjøtre | 3 | -1,00 |
| Viftesvamp | 4 | 0,11 |
4 - Oppsummering
Denne studien dokumenterer utvikling og anvendelse av en artsspesifikk protokoll for analyse av lysosomal membranstabilitet (LMS) hos utvalgte bunnarter samlet inn nær et oppdrettsanlegg og i referanseområder. Totalt ble sju ROV-dykk gjennomført, med prøvetaking både nær oppdrettslokaliteten Anevik og i referanseområder. Prøvetakingsinnsatsen varierte mellom arter og lokalitetstyper, og flere arter var representert med et begrenset antall prøver.
LMS-resultatene viste tydelige artsforskjeller og indikerte for enkelte arter lavere LMS nær oppdrettsanlegget sammenlignet med referanseområder, særlig for bergskjell og viftesvamp. Andre arter, som kålrabisvamp, viste høy LMS uavhengig av lokalitetstype. Resultatene antyder at LMS kan være følsom for lokal miljøpåvirkning hos enkelte arter, men tolkningen begrenses av lave prøvetall.
Visuell helse var generelt dårligere hos prøver samlet nær oppdrettsanlegget sammenlignet med referanseområder. Dette mønsteret var konsistent for flere arter, men variasjonen innen arter var betydelig, og enkelte arter var representert med få prøver.
Sammenhengen mellom LMS og helseindeks var overveiende negativ for de fleste arter, noe som indikerer at høyere andel stabile celler ofte sammenfaller med bedre visuell helse. Korrelasjonene var imidlertid av varierende styrke og basert på små datasett, og resultatene må derfor tolkes med forsiktighet.
Samlet viser studien at LMS-metoden er gjennomførbar for flere bunnarter og har potensial som indikator på fysiologisk tilstand i miljøovervåking. Samtidig understreker resultatene behovet for økt prøvetakingsomfang og videre metodisk standardisering før sikre konklusjoner om påvirkning fra oppdrett kan trekkes.
5 - Takk
Forfatterne takker ROV-operatørene Sindre Nygård Larsen og Sverre Waardal Heum, fartøyinstrument Reidar Johannesen, mannskapet på PIA og prosjektteamet for deres bidrag og støtte under toktet. Takk til FHF for finansiering (VDWS Transition, prosjektnr 901785).
6 - Referanser
Edge, K. J., Dafforn, K. A., Simpson, S. L., Roach, A. C., og Johnston, E. L. 2014. A biomarker of contaminant exposure is effective in large scale assessment of ten estuaries. Chemosphere, 100: 16–26. https://www.sciencedirect.com/science/article/pii/S0045653514000356.
Edge, K. J., Dafforn, K. A., Simpson, S. L., Ringwood, A. H., og Johnston, E. L. 2015. Resuspended contaminated sediments cause sublethal stress to oysters: A biomarker differentiates total suspended solids and contaminant effects. Environmental Toxicology and Chemistry, 34: 1345–1353. https://doi.org/10.1002/etc.2929.
Edge, K. J., Johnston, E. L., Dafforn, K. A., Simpson, S. L., Kutti, T., og Bannister, R. J. 2016. Sub-lethal effects of water-based drilling muds on the deep-water sponge Geodia barretti. Environmental Pollution, 212: 525–534. https://www.sciencedirect.com/science/article/pii/S0269749116301737.
Kutti, T., Legrand, E., Husa, V., Olsen, S. A., Gjelsvik, Ø., Carvajalino-Fernandez, M., og Johnsen, I. A. 2022. Fish farm effluents cause metabolic depression, reducing energy stores and growth in the reef-forming coral Lophelia pertusa. Aquaculture Environment Interactions, 14: 279–293. https://www.int-res.com/abstracts/aei/v14/p279-293/.
Lowe, D. M., Moore, M. N., og Evans, B. M. 1992. Contaminant impact on interactions of molecular probes with lysosomes in living hepatocytes from dab Limanda limanda. Marine Ecology Progress Series, 91: 135–140. http://www.jstor.org/stable/24832651.
Mamaca, E., Bechmann, R. K., Torgrimsen, S., Aas, E., Bjørnstad, A., Baussant, T., og Floch, S. L. 2005. The neutral red lysosomal retention assay and Comet assay on haemolymph cells from mussels (Mytilus edulis) and fish (Symphodus melops) exposed to styrene. Aquatic Toxicology, 75: 191–201. https://www.sciencedirect.com/science/article/pii/S0166445X05002596.
Mukherjee, S., Ray, M., Dutta, M. K., Acharya, A., Mukhopadhyay, S. K., og Ray, S. 2015. Morphological alteration, lysosomal membrane fragility and apoptosis of the cells of Indian freshwater sponge exposed to washing soda (sodium carbonate). Ecotoxicology and Environmental Safety, 122: 331–342. https://www.sciencedirect.com/science/article/pii/S0147651315300579.
Ringwood, A. H., Conners, D. E., og Hoguet, J. 1998. Effects of natural and anthropogenic stressors on lysosomal destabilization in oysters Crassostrea virginica. Marine Ecology Progress Series, 166: 163–171. https://www.int-res.com/abstracts/meps/v166/meps166163.
Ringwood, A. H., Conners, D. E., Hoguet, J., og Ringwood, L. A. 2005. Lysosomal destabilization assays for estuarine organisms. In Techniques in Aquatic Toxicology, Volume 2, 1st Edition, pp. 287–300. Red. G. K. Ostrander. CRC Press.
Strand, R., Whalan, S., Webster, N. S., Kutti, T., Fang, J. K. H., Luter, H. M., og Bannister, R. J. 2017. The response of a boreal deep-sea sponge holobiont to acute thermal stress. Scientific Reports, 7: 1660. https://doi.org/10.1038/s41598-017-01091-x.
7 - Vedlegg
7.1 - Vedlegg A1
| ROV-dykke nr | Dato | Område | Vitenskapelig navn | Vanlig navn | Prøvenummer | Bruk | Dybbe (m) | Breddegrad | Lengdegrad | Kommentar |
|---|---|---|---|---|---|---|---|---|---|---|
| 356 | 16-08 | Referanse | Primnoa resedaeformis | Risengrynkorall | 501 | LMS | 401 | 67,990 | 15,303 | Brukt til testing av LMS-forhold |
| 356 | 16-08 | Referanse | Primnoa resedaeformis | Risengrynkorall | 502 | 378 | 67,990 | 15,302 | TAPT | |
| 356 | 16-08 | Referanse | Paragorgia arborea | Sjøtre | 503 | LMS | 378 | 67,990 | 15,302 | |
| 356 | 16-08 | Referanse | Paragorgia arborea | Sjøtre | 504 | LMS | 354 | 67,990 | 15,302 | Brukt til testing av LMS-forhold |
| 356 | 16-08 | Referanse | Paragorgia arborea | Sjøtre | 505 | LMS | 341 | 67,990 | 15,301 | |
| 356 | 16-08 | Referanse | Primnoa resedaeformis | Risengrynkorall | 506 | 343 | 67,990 | 15,301 | TAPT | |
| 356 | 16-08 | Referanse | Phakellia ventilabrum | Viftesvamp | 507 | LMS | 342 | 67,990 | 15,301 | Brukt til testing av LMS-forhold |
| 356 | 16-08 | Referanse | Phakellia ventilabrum | Viftesvamp | 508 | 337 | 67,990 | 15,301 | TAPT | |
| 356 | 16-08 | Referanse | Phakellia ventilabrum | Viftesvamp | 509 | 319 | 67,989 | 15,300 | TAPT | |
| 356 | 16-08 | Referanse | Acesta excavata | Bergskjell | 510 | LMS | 316 | 67,989 | 15,300 | |
| 356 | 16-08 | Referanse | Acesta excavata | Bergskjell | 511 | LMS | 394 | 67,990 | 15,303 | Brukt til testing av LMS-forhold |
| 356 | 16-08 | Referanse | Acesta excavata | Bergskjell | 512 | LMS | 394 | 67,990 | 15,303 | |
| 356 | 16-08 | Referanse | Acesta excavata | Bergskjell | 513 | LMS | 394 | 67,990 | 15,303 | |
| 356 | 16-08 | Referanse | Primnoa resedaeformis | Risengrynkorall | 514 | LMS | 394 | 67,990 | 15,303 | Prøve løsnet fra havbunnen |
| 357 | 16-08 | Referanse | Geodia barretti | Kålrabisvamp | 515 | LMS | 349 | 67,988 | 15,350 | Brukt til testing av LMS-forhold |
| 357 | 16-08 | Referanse | Geodia barretti | Kålrabisvamp | 516 | LMS | 349 | 67,988 | 15,350 | |
| 357 | 16-08 | Referanse | Geodia barretti | Kålrabisvamp | 517 | LMS | 329 | 67,988 | 15,351 | |
| 357 | 16-08 | Referanse | Phakellia ventilabrum | Viftesvamp | 518 | LMS | 310 | 67,988 | 15,351 | |
| 357 | 16-08 | Referanse | Phakellia ventilabrum | Viftesvamp | 519 | LMS | 299 | 67,988 | 15,351 | |
| 357 | 16-08 | Referanse | Primnoa resedaeformis | Risengrynkorall | 520 | LMS | 299 | 67,988 | 15,351 | |
| 357 | 16-08 | Referanse | Desmophyllum pertusum | Øyekorall | 521 | LIVE EXPERIMENTS | 275 | 67,988 | 15,351 | |
| 358 | 16-08 | Referanse | Desmophyllum pertusum | Øyekorall | 522 | LIVE EXPERIMENTS | 361 | 67,988 | 15,350 | |
| 358 | 16-08 | Referanse | Desmophyllum pertusum | Øyekorall | 523 | LIVE EXPERIMENTS | 356 | 67,988 | 15,350 | |
| 358 | 16-08 | Referanse | Desmophyllum pertusum | Øyekorall | 524 | LIVE EXPERIMENTS | 356 | 67,988 | 15,350 | |
| 359 | 17-08 | Nær anlegg | Geodia barretti | Kålrabisvamp | 525 | LMS | 320 | 68,003 | 15,269 | |
| 359 | 17-08 | Nær anlegg | Primnoa resedaeformis | Risengrynkorall | 526 | LMS | 303 | 68,003 | 15,269 | |
| 359 | 17-08 | Nær anlegg | Primnoa resedaeformis | Risengrynkorall | 527 | LMS | 303 | 68,003 | 15,269 | |
| 359 | 17-08 | Nær anlegg | Geodia barretti | Kålrabisvamp | 528 | LMS | 304 | 68,003 | 15,269 | |
| 359 | 17-08 | Nær anlegg | Primnoa resedaeformis | Risengrynkorall | 529 | LMS | 300 | 68,003 | 15,269 | |
| 359 | 17-08 | Nær anlegg | Geodia barretti | Kålrabisvamp | 530 | LMS | 305 | 68,003 | 15,269 | |
| 359 | 17-08 | Nær anlegg | Phakellia ventilabrum | Viftesvamp | 531 | LMS | 251 | 68,003 | 15,269 | |
| 360 | 17-08 | Nær anlegg | Acesta excavata | Bergskjell | 532 | LMS | 302 | 68,003 | 15,269 | |
| 360 | 17-08 | Nær anlegg | Acesta excavata | Bergskjell | 533 | LMS | 301 | 68,003 | 15,269 | |
| 360 | 17-08 | Nær anlegg | Acesta excavata | Bergskjell | 534 | LMS | 300 | 68,003 | 15,269 | |
| 360 | 17-08 | Nær anlegg | Acesta excavata | Bergskjell | 535 | LMS | 302 | 68,003 | 15,269 | |
| 361 | 17-08 | Nær anlegg | Phakellia robusta | NA | 536 | LMS | 281 | 68,002 | 15,269 | |
| 361 | 17-08 | Nær anlegg | Phakellia robusta | NA | 537 | LMS | 282 | 68,002 | 15,269 | |
| 361 | 17-08 | Nær anlegg | Paragorgia arborea | Sjøtre | 538 | LMS | 277 | 68,002 | 15,269 | |
| 361 | 17-08 | Nær anlegg | Paragorgia arborea | Sjøtre | 539 | LMS | 280 | 68,002 | 15,269 | |
| 361 | 17-08 | Nær anlegg | Paragorgia arborea | Sjøtre | 540 | LMS | 281 | 68,002 | 15,269 | |
| 362 | 17-08 | Referanse | Desmophyllum pertusum | Øyekorall | 541 | LIVE EXPERIMENTS | 357 | 67,988 | 15,350 | |
| 362 | 17-08 | Referanse | Desmophyllum pertusum | Øyekorall | 542 | LIVE EXPERIMENTS | 358 | 67,988 | 15,350 | |
| 362 | 17-08 | Referanse | Desmophyllum pertusum | Øyekorall | 543 | LIVE EXPERIMENTS | 361 | 67,988 | 15,350 |
7.2 - Vedlegg A2
A. Vevscelledissosiasjon og preparering:
-
Oppbevar dyret i kaldt sjøvann og i mørke.
-
I en 24-brønners cellekulturplate, tilsett 1 mL kald CMFS til hver brønn.
-
Vevspreparering:
| Art | Vevsforberedelse |
|---|---|
| Svamper | Kutt vevet i mindre biter (~ 1 cm) på et objektglass. |
| Risengrynkorall | Knus vevet (~1 cm) ved hjelp av morter og pistill. |
| Sjøtre | Kutt vevet i mindre biter (~ 1 cm) på et objektglass. |
| Bergskjell | Bruk sprøyte og kanyle til å samle 50 µL hemolymfe. Fjern kanylen før det oppsamlede volumet tømmes i et 1,5 mL rør. Hold prøven kald. Gå direkte til seksjonen Nøytralrød-assay. |
-
Plasser det homogeniserte vevet i én av brønnene i cellekulturplaten.
-
Inkuber platen tildekket med aluminiumsfolie i 30 minutter på kaldt underlag (kjøleskap eller is).
-
Skjær forsiktig prøvene med en Pasteur-pipette (med avknekt spiss) ved å forsiktig suge opp og slippe løsningen for å hjelpe celle dissosiasjon (ca. 20 ganger).
-
Overfør løsningen til et rør med kommersielle cell strainere med følgende størrelser:
| Art | Porestørrelse |
|---|---|
| Svamper | 40 µm |
| Risengrynkorall | 100 µm |
| Sjøtre | 70 µm |
-
Vent til væsken har passert gjennom filteret.
-
Sentrifuger prøvene (i felt, ca. 15 °C) ved 2000 g i 5 minutter.
-
Kast supernatanten, resuspender pelleten i 1 mL kald CMFS og sentrifuger (ca. 15 °C) ved 2000 g i 5 minutter.
-
Kast supernatanten og resuspender cellene i 50 µL CMFS (Merk: for sjøtre tilsett 150 µL CMFS).
B. Nøytralrød-assay:
-
Tilsett 50 µL NR-arbeidsløsning til prøven. (Merk: for sjøtre tilsett 150µL CMFS og for kålrabisvamp 100 µL CMFS).
-
Bland prøven med plastpipettespiss og oppbevar i lysbeskyttet kammer ved romtemperatur (ca. 15 °C) i 60 minutter.
-
Bland løsningen og plasser 20 µL på et objektglass rett før vurdering.
C. Cellevurdering: Vurder minst 50 celler per prøve i mikroskop ved bruk av 40×-objektiv, og registrer om fargestoffet er lokalisert i lysosomene eller i cytosol. Kun celler som inneholder lysosomer skal inkluderes i vurderingen.